QUMAS EQMS
クラウドベースのエンタープライズ・クオリティ・マネジメント
自動化された動的なワークフロー
グローバルな規制を遵守して新製品をできるだけ早く上市するためには、情報の収集、追跡、分析、および関連する問題の解決を管理するビジネス・プロセスを標準化し、自動化する必要があります。BIOVIA QUMAS EQMS は、企業の品質およびプロセス管理のクラウドベース・ソリューションであり、バリデーション済みの QMS 環境で規制、品質、コンプライアンス管理機能を包括的に統合して提供します。
BIOVIA QUMAS EQMS は、以下のような最も一般的な品質維持活動を対象としたプロセス管理機能により、組織全体で品質管理(QC)をサポートしています。CAPA、逸脱、変更管理、顧客のクレームおよび監査。自動化されたフォーム、ビジネス・ルール、動的なワークフロー・エンジンを備えた 1 つのインターフェースから、これらの各プロセスや追加のプロセスのワークフローを作成、レビュー、処理、承認することができます。
ユーザーの実績
-
逸脱と CAPA が 10~20% 減少
-
品質情報処理が 20~30% 迅速化
-
承認時間が 80% 短縮
-
年間 1,575 時間以上を節約
-
年間 670 万ユーロを節約
企業の品質およびプロセス管理
BIOVIA QUMAS は、逸脱、CAPA、変更管理、品質情報、監査など、QMS に関する部門の様々な事前設定された品質プロセスが用意され、レビュー、処理、承認、管理するために使用できます。
QUMAS のデータ中心のアプローチにより、品質コンテンツを柔軟に管理し、すべての品質データを再利用することができ、品質を包括的に把握できます。
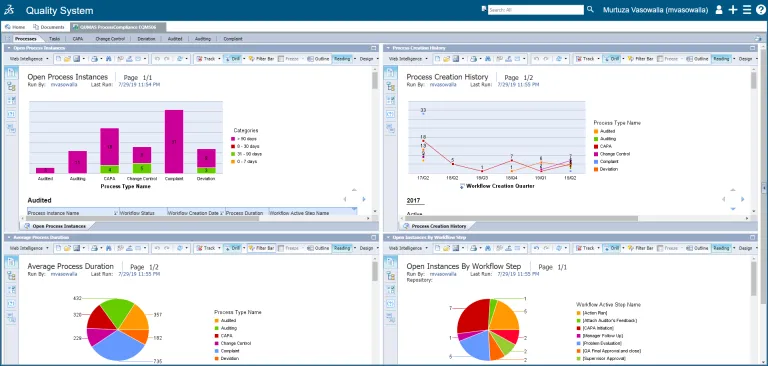
QUMAS のインタラクティブなダッシュボードは、ビジネス領域および品質業務に関する QMS の概要を提供します。レポートをエクスポート、電子メールで送付、スケジューリングすることができます。
QUMAS は、FDA 21 CFR Parts 11; 210; 820; 600、ISO 9000 および 14000 Standards、EU Annex 11 および cGxP Practices など、最も厳格な要件に対応します。
QUMAS は、QMS に関わる各部門がクラウド上で安全に、効率的に、かつコンプライアンスを遵守した情報交換を可能にします。
MyQUMAS と呼ばれる 1 つのユーザーフレンドリーなインターフェースから、すべての品質およびコンプライアンス機能にアクセスすることができ、コンプライアンスに関するコンテンツ、プロセス、タスクを簡単に共有することができます。
品質に関連する事項
QUMAS EQMS を使用すると、効果的な CAPA プロセス管理を作成し、複数の工場間での逸脱から生じる CAPA を追跡して対処することができます。 開始から完了まで、QUMAS は発見、記録、回覧、完了と承認の検証を CAPA プロセスの各ステップを監査しながら行います。クローズドループ・アプローチにより、自動データ入力、別のフォームから直接 CAPA フォームの起動、根本原因へのリンク、影響を受ける SOP の更新を同じソリューション内で行うことができます。
QUMAS EQMS を使用すると、関連する SOP に従って、すべての逸脱を記録、回覧、分析し、正確に対応することができます。管理されたドキュメントを添付して、根本原因の解析中に CAPA を開始し、傾向に対する知見を得ることもできます。
QUMAS EQMS により、変更管理プロセスを簡素化して効率的に管理し、製品およびプロセスの変更が機能にどのように影響するか評価できます。プロジェクトの評価、計画、構築、実装、検証、終了の変更管理プロセスを自動化することで、QUMAS は FDA 規制(21 CFR Parts 210、820、600)および ISO 規格(9000、1400 など)への準拠を推進します。有効性レビューは、変更管理が目標を満たしたかを確認できます。変更管理の傾向レポートでは、パターンと傾向の総合的なビューが示されます。
QUMAS EQMS により、すべての品質情報を追跡、調査して、解決までの過程を追跡できます。このシステムは、必要なフォームの入力を自動化し、管理レポートを作成しながら、すべての品質情報を適切に評価するのに役立ちます。ある施設での品質情報の傾向分析は、他の施設での予防措置のきっかけとなり、同じ問題が再発防止に役立ちます。
QUMAS EQMS を使用することで、監査人が期待するスケジュールや法律によって求められる、すべての不適合、観察、勧告を記録、追跡、更新、解決することができます。このシステムは、GCP 要件を満たすための臨床試験の監査や、企業の品質基準に準拠しているかどうかのサプライヤーの監査、または ISO 9001 監査の準備のための内部部門の監査をサポートします。また、監査人がより効率的に監査を計画し、実行することができます。
さあ、始めましょう
医薬品の品質の世界は変化しています。BIOVIA で一歩先を行く方法を発見しましょう。
その他の情報
BIOVIA の活用方法
組織の規模の大小を問わず、シームレスなコラボレーションと持続可能なイノベーションに、このソリューションがどう役立つかについて、BIOVIA の担当技術者がご説明します。
始めましょう
学生、教育機関、専門家、企業向けのコースとクラスをご用意しています。お客様に最適な BIOVIA トレーニングを受講してください。
サポートを受ける
ソフトウェアやハードウェアの資格認定、ソフトウェアのダウンロード、ユーザー・マニュアル、サポート連絡先、サービス・オファリングに関する情報を入手できます。