监管管理
利用结构化内容重塑文档创作
实现监管提交的数据中心化、数字化和自动化
为了确保发起人能够准确、轻松地与全球相关监管机构共享内容并合作,监管信息管理至关重要。通过提供基于模型的数据驱动方法来自动生成这些关键内容,达索系统正在推动提交管理的转型。现在,我们能够从发起人的企业数据湖或单个系统中收集重要数据,并生成相关的 CMC 表格、图表和关键叙述。美国食品药品监督管理局 (FDA) 的 KASA 等措施意味着,该行业现在必须充分利用人工智能,摆脱传统的从实验室系统逐词逐句剪切粘贴的做法。
我们的 CMC 创作解决方案不仅可提供数据,而且还能确保数据来源完全可追溯到源头、提供动态刷新数据的能力、在不同地区/提交之间重用内容、所有内容元素的完整“使用位置”、团队之间的实时协作,以及对 CMC 和其他提交模块进行变更控制和更新的无与伦比的能力。这款完全合格的 Saas 解决方案采用了先进的AI和结构化内容创作技术。
BIOVIA 监管管理软件的主要优势
合规性
减少手动操作导致的错误,确保数据和文档的一致性和完整性,确保数据的可追溯性和“设计的数据完整性”,满足 FDA、EMA 等机构的要求(包括数据格式),并减少提交后的问题
时间和预算
减少手动步骤和非增值任务,减少每个申请数据的手动查询,消除重复的数据验证审批,缩短审查周期并加快对相关机构的响应时间
协作
消除多个系统的复杂性,同时协作处理文档,基于结构化内容共享知识,规范和协调内部实践,并整合新的合作伙伴、供应商和客户
SaaS 云解决方案
BIOVIA 监管信息管理解决方案可在 3DEXPERIENCE 平台上获得,帮助实现以数据为中心、AI驱动的监管提交文件自动生成的优势。
主要优势:
- 通过消除手动传输(复制和粘贴),加速文档制作
- 通过自动生成文档,获得准确的报告
- 通过可追溯性和直接访问源数据,最大限度地提高透明度
- 通过安全的云端协作环境,保护知识产权
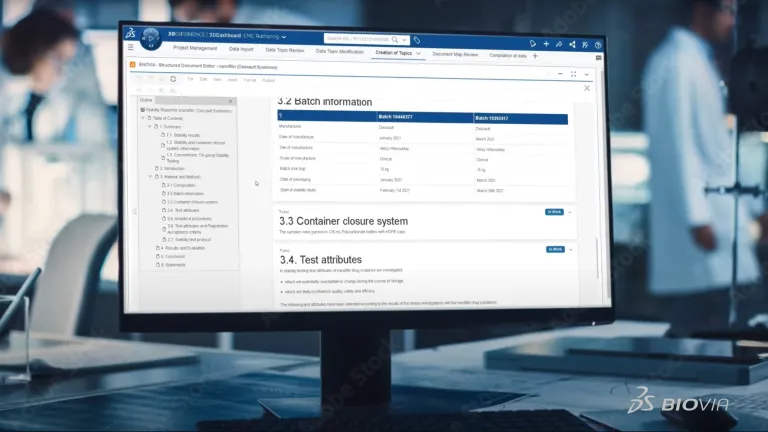
转变 CMC 档案创建
通过转向以数据为中心的 CMC 档案创建方法,简化文档创建。BIOVIA 结构化文档创作通过标准化格式、自动内容更新和安全协作,减少了与文档创建相关的时间和成本。
关于生命科学领域监管信息管理系统的常见问题答疑
监管信息管理 (RIM) 系统涉及收集、组织和维护合规性相关数据,以确保公司遵守相关法律法规。 它包括跟踪监管要求、文档管理以及向监管机构提交文件的流程,确保及时准确地遵守法规。
监管信息管理系统 (RIMS) 通过集中监管数据、优化提交和更新公司的监管变化来提高合规性。这可确保准确、及时地遵守全球法规,最大限度地减少错误和延误。
RIMS通过自动跟踪监管提交和截止日期,并提供有效的文档管理和合规警报工具,从而降低不合规风险。这有助于医疗保健组织避免受到处罚,并保持运营连续性。
RIM系统专为合规性管理而量身定制,提供用于跟踪监管提交、与监管机构集成以及提供高级安全和审计功能等特定功能。传统的文档管理系统则侧重于一般文档存储和检索,而不具有专门的监管功能。
了解更多
了解 BIOVIA 可以为您做些什么
与 BIOVIA 专家进行交谈,了解我们的解决方案如何在各种规模的企业中实现无缝协作和可持续创新。
了解更多内容
学生、学术界人士、专业人员和企业人员均可参加相关课程并加入班级。查找适合您的 BIOVIA 培训。
获取帮助
查找有关软硬件认证、软件下载、用户文档、支持联系人和服务项目的信息